
文章链接:https://onlinelibrary.wiley.com/doi/abs/10.1002/adfm.202210406
在过去的几十年里,抗生素的过度使用或滥用导致了严重的健康问题。研制没有抗菌耐药性和其他副作用的新型抗菌材料以取代抗生素,已成为一个迫在眉睫的问题,特别是针对革兰氏阴性菌的抗菌材料。纳米黏土是抗微生物耐药性应用的重要材料,它们有几个吸引人的特点:价格便宜,数量丰富,最重要的是,它们在很长一段时间内被用于医疗。纳米黏土可以杀死细菌且没有任何抗菌素耐药性,但迄今为止只有大约10%的纳米黏土具有抗菌或抑菌性能,抗菌纳米黏土主要包括高岭石、蒙脱石、伊利石、累托石、叶蜡石、膨润土及其混合物。目前,天然纳米黏土抗菌作用的机理主要有:(1)释放有毒金属离子,如Cu2+、Mn2+、Zn2+等,以及黏土结构中溶解的Al3+;(2)金属离子芬顿反应;(3)直接接触杀菌。前两种机制的抑菌作用取决于金属离子在黏土中的溶解度和还原性,通过改变微环境的pH值和氧化状态来杀灭细菌。据报道,纳米黏土颗粒的大小、环境pH值和表面电荷、水化能力等因素都与其杀菌活性有关。但黏土直接接触杀菌的抑菌机制尚不清楚。
研究方案
众所周知,黏土矿物边缘面的酸碱化学性质比体相结构复杂得多,活性也更强。此外,黏土表面可以通过与脂多糖(LPS)之间的可逆结合抑制革兰氏阴性菌的生长,而且,富含高岭土的哥伦比亚亚马逊黏土中的溶解铝被证明可以杀死细菌。因此,基于不同黏土均含有Al-O,Si-O结构,我们推测具有Al-O结构的纳米黏土边缘面可能对抗菌性能起着重要作用。等离子体刻蚀后,片层结构上形成的孔洞显著增加了高岭石的边缘面。本研究通过实验和模拟相结合的方法,揭示了纳米黏土边缘表面对革兰氏阴性菌的抑菌机理。基于密度泛函理论和分子动力学(DFT/MD)计算,从原子水平阐明了天然黏土边缘表面在抗菌活性中的作用。大肠杆菌外膜与高岭石(110)和(1-10)表面具有强氢键和范德华力相互作用,吸附在高岭石表面使得大肠杆菌外膜发生折叠;大肠杆菌外膜LPS与高岭石(1-10)表面之间的质子耦合电子转移,亦可破坏大肠杆菌外膜结构。最后通过这两种方式协同作用,高岭石边缘面将大肠杆菌杀死。考虑到大部分黏土矿物均具有Al-O结构,该研究对黏土矿物的抗菌应用提供了新的思路。
此外,天然纳米黏土和纳米黏土矿物基材料最重要的抗菌机制之一是通过产生的•OH有效杀死大肠杆菌细胞。但•OH存在时间较短,且只能扩散至数纳米范围,这就需要•OH发生在靠近细菌表面的地方才能对细菌进行有效攻击。当高岭石或其他纳米黏土的带更多正电荷的边缘面增多时,一方面,大肠杆菌细胞可以直接被带有活性的Al-(OH)和Al-(OH2)基团接触杀死;另一方面,大肠杆菌在纳米黏土边缘表面的吸附会大大增加细菌与•OH接触的概率而提升抗菌效果。这些结果不仅对天然纳米黏土抗菌作用提供了新的证据,而且对纳米黏土基抗菌材料作为现有抗生素和抗菌剂的安全替代品的未来发展也具有重要意义。
研究成果
1. 高岭石抗菌材料的制备和抗菌实验
与具有六边形层状结构的高岭石相比,经等离子体处理后E-Kaol的层状结构上出现了大量的孔洞。通过边缘质子化,E-Kaol边缘面具有更多正电荷。原始高岭石几乎没有任何抗菌活性,而经过等离子体处理后的E-Kaol能够杀死大多数大肠杆菌(E. coli)细胞。TEM图像显示,经E-Kaol30处理后大肠杆菌外膜(OM)有明显受损。用NMR和DFT计算对E-Kaol30中Al的配位环境进行了表征,边缘面的Al-(OH)和Al-(OH2)具有较强活性。

图1 (a)
Kaol的TEM, AFM 图,以及E. coli与Kaol相互作用4 h的TEM图 (从上到下)。(b)
E-Kaol30的TEM,
AFM 图,以及E. coli与E-Kaol30相互作用4 h的TEM图 (从上到下)。图中黑色箭头表示E. coli外膜被破坏。(c)Kaol和E-Kaol抗菌结果。(d)高岭石的不同边缘面结构示意图。

图2 (a) Kaol和E-Kaol30的NMR结果,(b) DFT计算的高岭石的不同类型脱水能。
2. 高岭石边缘面与大肠杆菌外膜的界面相互作用
FTIR和XPS结果均证实大肠杆菌外膜的羧基、磷酸基团与E-Kaol30之间存在界面结合作用,且其表面的磷酸基被破坏并游离。
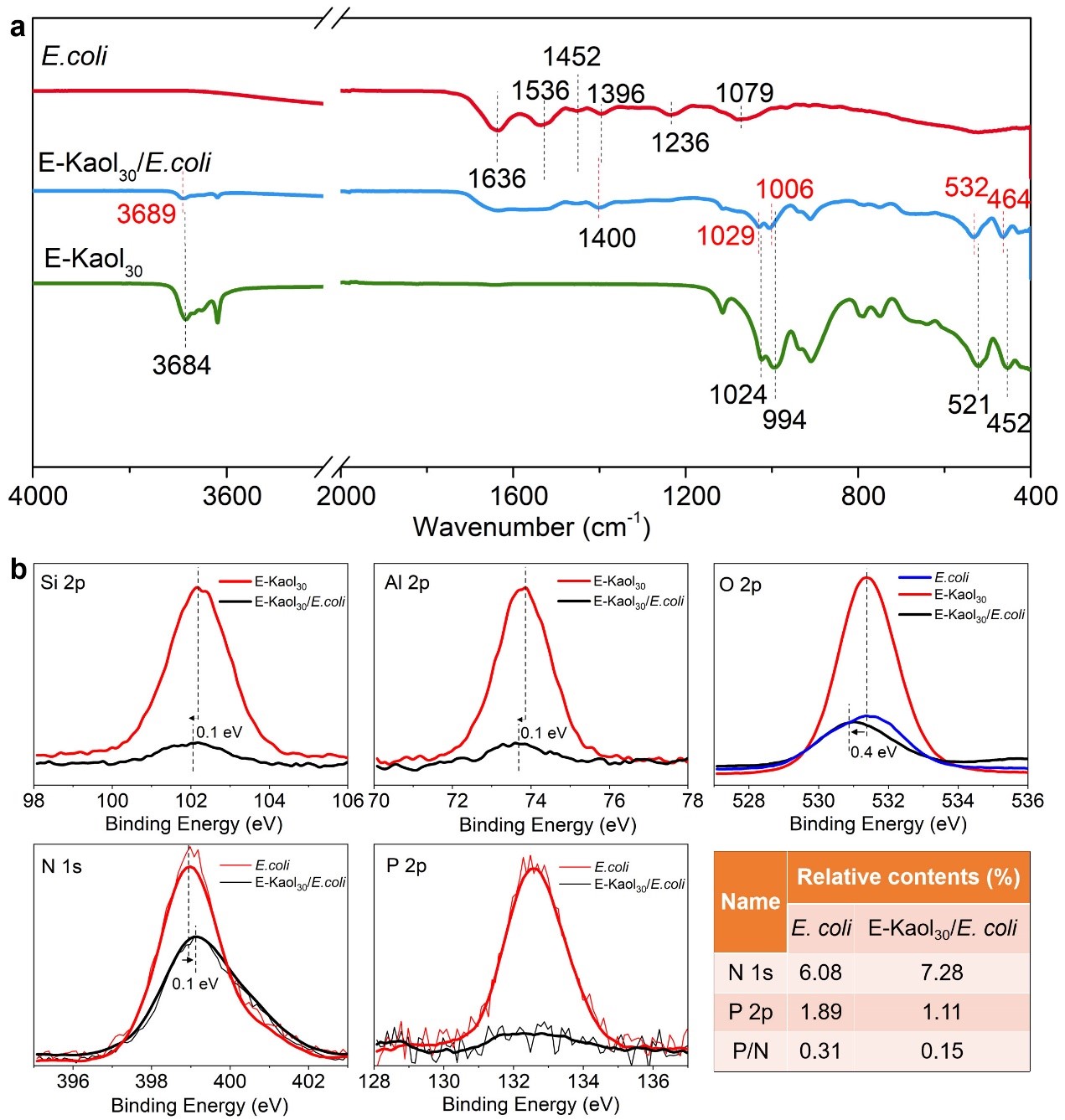
图3 Kaol和E-Kaol30 的(a) FTIR和(b) XPS结果。
3 高岭石边缘面抗菌机理
计算模拟可以用来研究高岭石边缘面与大肠杆菌外膜在原子水平上的相互作用机理。通过分子动力学模拟研究了LPS与高岭石边缘面相互作用的动力学过程。LPS与高岭石边缘面具有很强的氢键结合,其中磷酸基团与高岭石边缘面之间的相互作用尤其强。吸附后,外膜受到的张力作用可能是引起细菌机械变形、细胞破裂和死亡的原因,这种现象类似于“磷脂海绵效应”的接触-杀伤机制,其抗菌作用是通过细菌细胞膜上带负电荷的磷脂选择性粘附到纳米黏土的正极表面而发生。通过DFT计算进一步观察到高岭石边缘面两种不同的抑菌机理:一种是K1和L1都能吸附在(110)和(1-10)表面,具有强氢键和范德华力。另一个机制是通过质子耦合电子转移(PCET),E-Kaol30的(1-10)表面可以破坏大肠杆菌外膜,从而杀死大肠杆菌,具体来说,磷酸基团的质子会被转移到高岭石(1-10)表面的Al-(OH)和Al-(OH2)结构上。
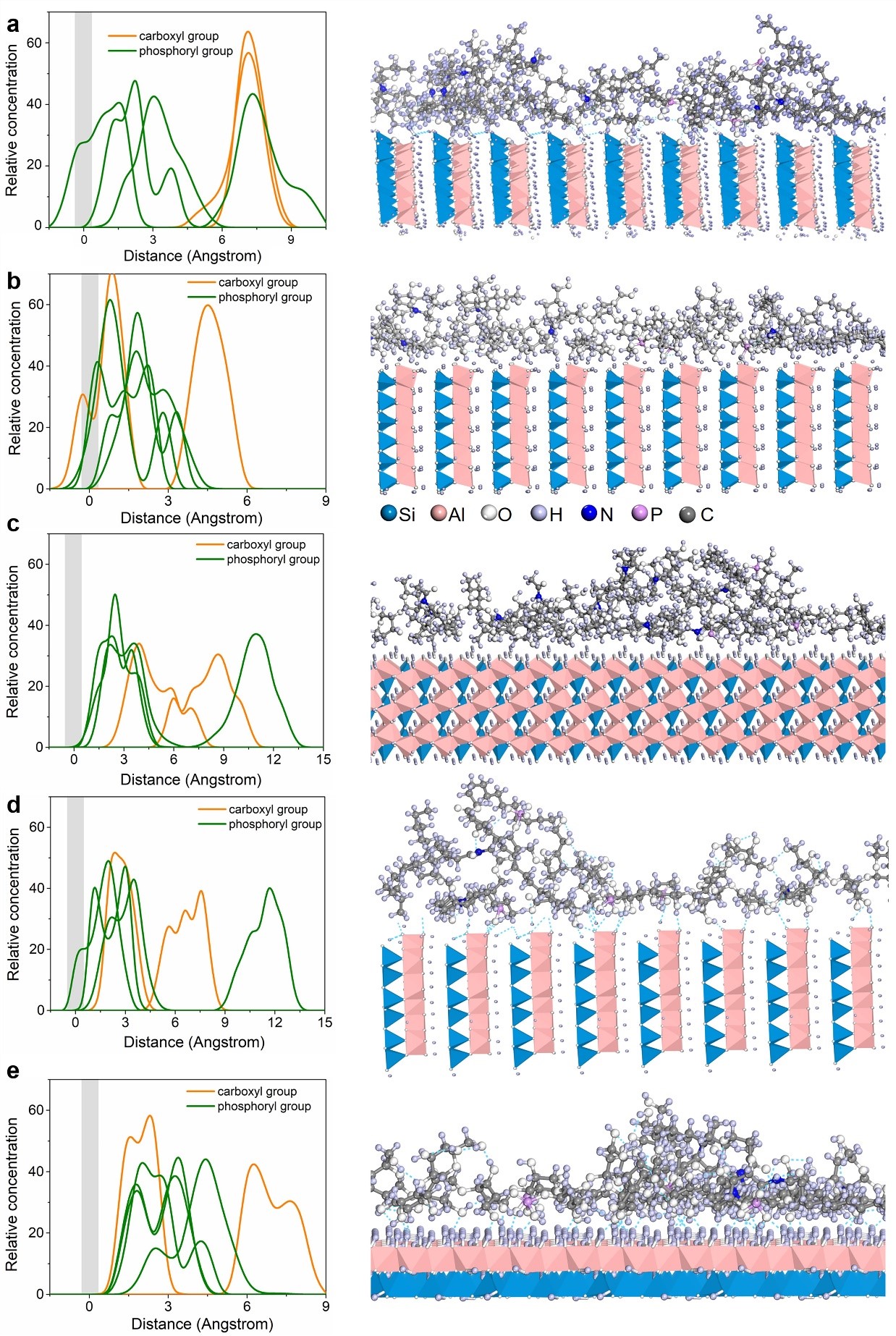
图4 LPS在高岭石(110), (100), (1-10), (010)和(1-13) 面(a-e)的相互作用分子动力学图。

图5 S1-S5(分别对应a-e)在高岭石边缘面的吸附能。(f) S1-S5在高岭石边缘面的最小吸附能。 (g, h) K1和L1在高岭石边缘面的吸附能。(i) K1和L1在高岭石边缘面的最小吸附能。

图6 L1在高岭石(110)表面形成的(a)氢键以及(c)界面之间的电荷密度图。K1在高岭石(110) 表面形成的(b)氢键以及(d)界面之间的电荷密度图。L1在高岭石(1-10)表面形成的(e)氢键以及(g)界面之间的电荷密度图。K1在高岭石(1-10)表面形成的(f)氢键以及(h)界面之间的电荷密度图。
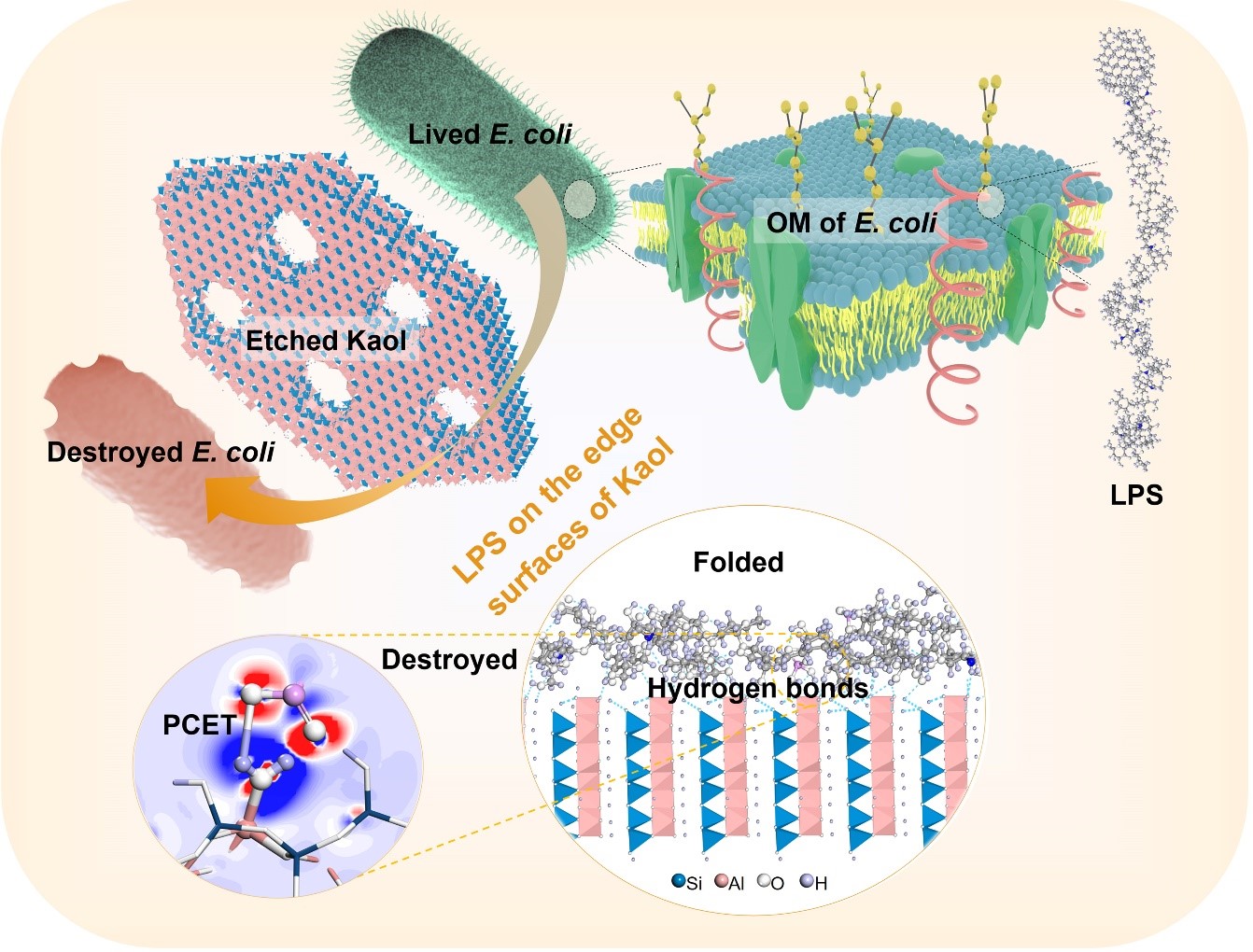
图7 E-Kaol30抗菌机理示意图。